Cat. No. / ID: 34362
특징
- TAGZyme 효소에 의한 제거에 최적화된 발현된 His-tag
- 효율적인 His-tag 제거: 37°C에서 단 30분 안에 >95% 달성
- N-말단 His-tagged 단백질의 고수준 발현
- 고순도 최종 산물
- Ni-NTA 방식으로 오염 물질을 완전히 제거
제품 세부 정보
TAGZyme Enzyme DAPase는 최대 10mg의 His-tagged 단백질에서 매우 특이적이고 효율적으로 His-tag를 제거할 수 있는 충분한 효소를 포함하고 있습니다. TAGZyme System은 TAGZyme pQE-2 벡터를 사용하여 발현된 고유한 DAPase 중지 시점을 포함하는 단백질에서 His-tag를 제거하는 데 사용할 수 있습니다.
성능
TAGZyme DAPase Enzyme은 TAGZyme pQE-2 벡터를 사용하여 발현된 '중지 시점'까지 N-말단 His tag에서 디펩티드를 순서대로 효율적으로 제거합니다.
원리
His-tagged 재조합 단백질은 단백질 구조와 기능을 연구하는 데 유용한 도구가 되었습니다. His tag는 크기가 작고 면역원성이 낮기 때문에 일반적으로는 제거할 필요가 없습니다. 그러나 X-선 또는 NMR을 이용한 구조 결정 연구 또는 치료제 생산과 같은 일부 애플리케이션에서는 벡터 유래 아미노산이 없는 단백질 제품이 선호됩니다.
TAGZyme pQE-2 벡터는 내재적 DAPase 중지 시점이 포함된 단백질에 적합합니다.
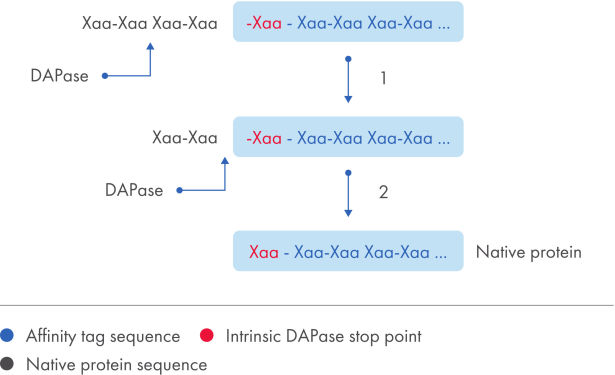
TAGZyme System은 높은 특이성과 효율성으로 재조합 단백질에서 N-말단 His tag를 제거합니다. DAPase 효소는 정제된 His-tagged 단백질의 N-말단에서 디펩티드를 순차적으로 절단하는 데 사용됩니다(그림 'His-tag 제거' 참조). 효소가 기질로 작용할 수 없는 아미노산 모티프인 '중지 시점'에 도달하면 소화가 중단됩니다('DAPase 중지 시점' 표 참조).
DAPase 중지 시점
| 아미노산 | DAPase 중지 시점(↓) 염기서열* |
|---|---|
| 라이신(Lys, K) | Xaa-Xaa...Xaa-Xaa ↓ Lys-Xaa... |
| 아르기닌(Arg, R) | Xaa-Xaa...Xaa-Xaa ↓ Arg-Xaa... |
| 프롤린(Pro, P) | Xaa-Xaa...Xaa-Xaa ↓ Xaa-Xaa-Pro-Xaa... |
| 프롤린(Pro, P) | Xaa-Xaa...Xaa-Xaa ↓ Xaa-Pro-Xaa-Xaa... |
| 글루타민(Gln, Q)† | Xaa-Xaa...Xaa-Xaa ↓ Gln-Xaa... |
| 이소류신(Ile, I) | Xaa-Xaa...Xaa-Xaa ↓ Xaa-Ile-Xaa-Xaa... |
그림 참조
절차
고유한 중지 시점을 포함하는 재조합 단백질의 경우, TAGZyme pQE-2 벡터를 사용하여 발현하면 DNA 삽입물의 클로닝 부위에 관계없이 N-말단 His-tag를 완전하고 효율적으로 제거할 수 있습니다(그림 'His-tag 제거' 참조). DAPase 효소로 배양한 후 반응 혼합물을 Ni-NTA 매트릭스를 사용하여 감산 고정화 금속 친화성 크로마토그래피(Immobilized-Metal Affinity Chromatography, IMAC)를 실시합니다( '태그가 제거된 단백질의 정제' 그림 참조). His-tag 단편과 TAGZyme DAPase Enzyme(C-말단 6xHis tag를 운반)이 매트릭스에 결합하고, 흘러 지나가는 분획에서 tag가 제거된 순수 표적 단백질이 회수됩니다.
그림 참조
응용 분야
TAGZyme System은 특정 절단, 재조합 시약 사용 및 모든 오염 물질의 완전한 제거가 가능하므로, 다음과 같은 애플리케이션에서 His-tag가 없는 단백질을 생산하기 위해 선택되는 방법입니다.
- NMR 또는 X-선 결정학을 통한 단백질 구조 결정
- 치료용 단백질 생산
지원되는 데이터 및 수치
His-tag 제거.
TAGZyme 효소를 사용한 전체 절단 전략에 대한 개략적인 요약. 성숙한 표적 단백질을 얻기 위해 자연적인 중지 시점을 포함한 단백질에서 DAPase 효소가 N-말단 His tag를 절단.